
Статьи


Значение предсезонно-сезонной сублингвальной иммунотерапии при аллергическом риноконъюнктивите, индуцированном пыльцой растений
06.07.2022
Аннотация
|
Аллерген-специфическая иммунотерапия (АСИТ) представляет собой метод лечения респираторных аллергических заболеваний, в том числе вызванного пыльцой аллергического ринита (АР), который направлен на модификацию течения болезни и одобрен в современных терапевтических руководствах. Применяемые в настоящее время при АР, индуцированном пыльцой, схемы АСИТ можно подразделить на непрерывные (то есть круглогодичные) и прерывистые (в частности, предсезонные, сезонные или комбинированные предсезонно-сезонные). Предсезонно-сезонные схемы обычно применяются при проведении сублингвальной аллергенспецифической иммунотерапии (СЛИТ) и обладают экономическим преимуществом перед круглогодичными схемами, сопровождаясь также более высокой комплаентностью пациентов. Тем не менее эти преимущества не должны достигаться за счет меньшей эффективности или худших показателей безопасности. Результаты недавно проведенных двойных слепых плацебо-контролируемых рандомизированных клинических исследований показывают, что предсезонно-сезонная СЛИТ является безопасным и эффективным методом лечения пациентов с АР, индуцированного пыльцой трав (лечение осуществляется с помощью таблетированной лекарственной формы) или березовой пыльцой (для лечения применяется жидкая лекарственная форма). Прогресс в разработке СЛИТ основывается на определении оптимальной дозы основного аллергена, частоты введения (ежедневно), длительности предсезонной терапии (четыре месяца) и числе сезонов, в которые проводится лечение (не менее трех). Пострегистрационные исследования предсезонно-сезонных схем СЛИТ с использованием аллергенов пыльцы березы или трав в условиях реальной практики подтвердили эффективность и безопасность, отмеченные в клинических исследованиях. При лечении АР, индуцированного пыльцой, схемы предсезонно-сезонной СЛИТ по меньшей мере столь же эффективны и безопасны, как круглогодичные схемы СЛИТ, но при этом ассоциируются с меньшими затратами и хорошей комплаентностью пациентов. Хорошая комплаентность может означать, что предсезонно-сезонные схемы СЛИТ по сути своей более эффективны и безопасны, чем круглогодичный режим СЛИТ. Анализ предсезонно-сезонной прерывистых схем показал, что лекарственная форма, содержащая аллергены пыльцы пяти трав, с индексом реактивности (ИР), равным 300 (300 ИР), представляет собой единственную таблетированную форму СЛИТ, для которой программа клинической разработки подтвердила краткосрочную, устойчивую и посттерапевтическую эффективность. Ключевые слова: аллергический ринит, предсезонный, сезонный, сублингвальная иммунотерапия, пыльца, береза, травы. |
Аллергический ринит (АР) представляет собой хроническое воспалительное заболевание верхних дыхательных путей, индуцируемое аэроаллергенами и опосредованное иммуноглобулином Е (IgE), которым страдают до 30% взрослых людей и до 40% детей и которое вносит вклад в развитие бронхиальной астмы [1-3]. Аллергический конъюнктивит является сопутствующим заболеванием приблизительно у двоих из троих людей, страдающих пыльцевым АР. В настоящее время общепризнанным является представление об АР как значимом обременительном заболевании с выраженным социально-экономическим воздействием и отрицательным влиянием на связанное со здоровьем качество жизни, производительность труда и успеваемость в школе, качество сна, настроение и социальное функционирование [4-10]. Пыльца, образующаяся на опыляемых ветром растениях (в том числе травах, деревьях и сорной растительности) на протяжении одного или нескольких периодов продолжительностью от нескольких недель до нескольких месяцев ежегодно, является главным атопическим сенсибилизирующим агентом в популяции Европы и Северной Америки [11,12]. Сезонный АР характеризуется четкой связью с определенными периодами распространения пыльцы, даты начала и продолжительность которых различаются от года к году и зависят от географической и климатической зоны [13,14]. Например, продолжительность распространения пыльцы растений семейства мятликовых, зарегистрированная на 13 европейских станциях мониторинга, варьирует от 69 дней в Рейкьявике до 154 дней в Салониках [13]. Такие деревья, как береза (Betula), олива (Olea europaea) и кипарис (Cupressus sp.), также образуют высокоаллергенную пыльцу [14]. Длительность сезона пыления березы составляет от 38 дней в Рейкьявике до 107 дней в городе Леньяно (недалеко от Милана) [13]. Важно отметить, что экспозиция воздействия пыльцы (а следовательно, вероятность развития клинических проявлений заболевания у лиц с атопией) увеличивается в результате изменений климата: в некоторых регионах концентрация пыльцы выше, период ее распространения продолжительнее, а частота дождей меньше [14-16]
Аллерген-специфическая иммунотерапия (АСИТ) при АР, вызванном пыльцой растений
В большинстве случаев АР лечение осуществляется с использованием симптоматических противоаллергических препаратов (в частности, Н1-антигистаминных препаратов) и/или противовоспалительных препаратов (в частности, интраназальных кортикостероидов (ИнКС)) [1,2,17,18]. Однако приблизительно у 30% пациентов (большинство из которых страдают среднетяжелым АР) при помощи симптоматических препаратов не удается достичь достаточного контроля заболевания [19]. АСИТ представляет собой одобренный в методических руководствах способ лечения, направленный на модификацию течения болезни у пациентов с опосредованными IgE респираторными аллергиями [1,2,20-23]. Эффективность АСИТ в купировании симптомов по меньшей мере сопоставима с эффектом ИнКС [24,25]. Будучи методом лечения, направленным на модификацию течения болезни, АСИТ оказывает клинический эффект на протяжении периода до 12 лет [26,27] и уменьшает частоту повторных эпизодов сенсибилизации и аллергической астмы у пациентов с АР [28]. При АР эффективными оказываются как подкожная иммунотерапия (ПКИТ), так и сублингвальная иммунотерапия (СЛИТ), что подтверждено результатами крупномасштабных двойных слепых, плацебо-контролируемых рандомизированных клинических исследований (РКИ), метаанализов и данными согласительных документов [27,29-35]. Кроме того, препараты для СЛИТ могут назначаться в виде капель или таблетированных лекарственных форм [20,21,36-39]. Несмотря на доказанную краткосрочную и долгосрочную эффективность как ПКИТ, так и СЛИТ и десятилетия клинического опыта, до сих пор нет единого мнения по таким вопросам, как: 1) оптимальная доза десенсибилизирующего аллергена (это связано с малым количеством исследования подбора доз для растворов СЛИТ); 2) частота введения; 3) общая длительность лечения; 4) схема терапии и 5) сезонность АСИТ при пыльцевом АР [31,34].
Схемы введения препаратов при лечении АР, вызванного пыльцой растений
Схемы многолетнего лечения с использованием АСИТ (рисунок 1) можно подразделить на непрерывные (то есть круглогодичные) и прерывистые (когда терапия ежегодно прерывается на несколько месяцев).
За исключением фазы накопления аллергена (в течение которой на протяжении нескольких недель, дней или даже часов, в зависимости от того, используется ли стандартный, ускоренный или сверх-ускоренный протокол, осуществляется переход к введению поддерживающей дозы аллергена), ПКИТ обычно проводится в рамках непрерывной круглогодичной поддерживающей схемы, при которой инъекции выполняются в условиях медицинского учреждения с регулярными интервалами (при использовании экстрактов аэроаллергенов - обычно каждые 4-6 недель) на протяжении нескольких лет, а далее в течение нескольких периодов распространения пыльцы (рисунок 1) [22]). В двойных слепых рандомизированных плацебо-контролируемых исследованиях проведение инъекций с более длительными интервалами не изучалось. Данные литературы свидетельствуют о том, что риск тяжелых нежелательных реакций на ПКИТ с использованием пыльцевых аллергенов усиливается во время соответствующих периодов максимального распространения пыльцы [40]. Например, Lockey et al. при анализе данных, собранных с 1945 по 1973 гг., показали, что 41% из числа всех случаев смерти, связанной с ПКИТ, произошли в течение периода распространения пыльцы [41]. Таким образом, последние практические рекомендации по АСИТ в США подтверждают историческую практику и свидетельствуют о том, что уровень поддерживающей дозы может быть снижен (и, несомненно, не требует повышения) в течение тех периодов, когда пациент в силу естественных условий подвержен воздействию более высоких концентраций аллергена, вызвавшего заболевание [22,42,43] (рисунок 1).
Несмотря на доказанную эффективность ПКИТ, этот метод по-прежнему характеризуется многочисленными недостатками, относящимися к аспектам безопасности и простоты применения. Действительно, метод СЛИТ обладает преимуществами в плане безопасности и удобства использования (в особенности у детей) [20,21,44]. Для препаратов СЛИТ изучены предсезонно-сезонные и круглогодичные схемы, однако чаще всего используются варианты предсезонно-сезонной терапии (рисунок 1). В обзоре 2009 года, изучившем схемы проведения СЛИТ пыльцевыми аллергенами (в большинстве случаев с использованием капельной лекарственной формы) [45] указано три исследования с использованием чисто предсезонной схемы введения ([46]), три исследования чисто сезонной терапии ([47,48]), восемь исследований непрерывной или частично постсезонной терапии ([49]) и 27 исследований комбинированной предсезонно- сезонной терапии. Как показывает опыт, капли для пыльцевой СЛИТ назначаются ежедневно, через день или три раза в неделю.
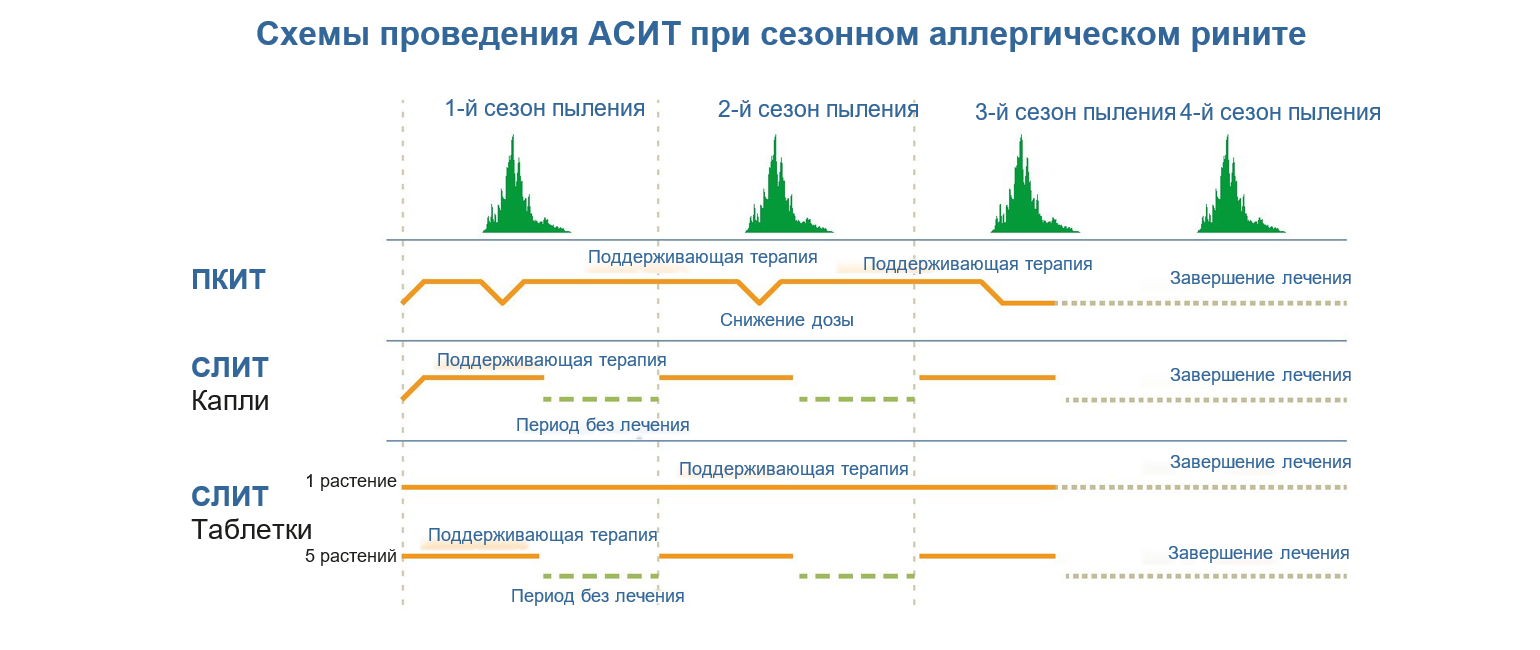
Рисунок 1. Режимы проведения АСИТ при сезонном аллергическом рините
При АР, вызванном пыльцой, постоянное или постсезонное проведение терапии проблематично, поскольку пациенты не ощущают пользы от СЛИТ после окончания сезона пыления (то есть в тот период, когда их симптомы исчезают). Продление периода применения препаратов ассоциируется с худшим уровнем комплаентности и, следовательно, меньшей вероятностью достижения эффекта [50,51].
Предсезонные и сезонные схемы терапии также имеют свои ограничения. В исследованиях таблетированной лекарственной формы СЛИТ препаратом на основе аллергена из смеси пыльцы 5 трав было показано, что 2-месячное предсезонное лечение (с последующей сезонной терапией) менее эффективно, чем 4-месячная предсезонная терапия [52,53]. Сходным образом в исследовании таблетированной лекарственной формы СЛИТ на основе одного вида растений было показано, что степень уменьшения выраженности симптомов риноконъюнктивита и оценки лечения возрастают по мере увеличения длительности предсезонной терапии (оптимальной, по-видимому, является 4-месячная длительность лечения) [54]. Таким образом, пациент, страдающий поллинозом и в течение многих лет соблюдающий режим предсезонно-сезонной терапии, должен помнить о необходимости приобретения лекарственных препаратов и начале лечения задолго до начала сезона пыления. Именно этой проблемы (соблюдения непрерывности лечения) удается избежать, строго придерживаясь круглогодичной схемы терапии. В исследовании, проведенном в Германии, частота возобновления рецептов (суррогатный показатель приверженности лечению) на СЛИТ или препараты для подкожной иммунотерапии была выше (на 55-71%), чем когда-либо отмечалось в случае применения обычных препаратов [55].
Многочисленные доказательства свидетельствуют в пользу безопасности и эффективности предсезонно-сезонной терапии пыльцевой аллергии с использованием капель СЛИТ при их назначении в течение одного или нескольких последовательных сезонов. Не так давно Worm et al. провели высокодоказательное двойное слепое плацебо-контролируемое РКИ, продолжавшееся в течение двух сезонов, в котором изучалась предсезонная и сезонная терапия сублингвальным раствором аллергенов пыльцы березы с индексом реактивности (ИР) 300 у 574 взрослых пациентов, ранее не получавших иммунотерапии и страдавших аллергическим риноконъюнктивитом на березовую пыльцу. Исследование проводилось в 56 научно-исследовательских центрах 11 европейских стран [56]. Лечение было начато за 4 месяца до ожидаемого сезона пыления. В начале исследования 68% пациентов имели поливалентную сенсибилизацию, у 20% наблюдалась легкая или среднетяжелая астма, у 54% - оральный аллергический синдром. Основная конечная точка для оценки эффективности (... в течение второго сезона пыления) оказалась значительно ниже (p<0,0001) в группе, получавшей активную СЛИТ (относительная разница с плацебо: 30,6%; разница между средними по методу наименьших квадратов (МНК): -2,04 [95% доверительный интервал: -2,69; -1,40]). Разница в первом сезоне пыления также составила 19,0% в пользу активной СЛИТ. Средний индекс использования лекарственных препаратов (medication score) в группе, применявшей СЛИТ с 300 ИР в обоих сезонах, был значительно ниже, причем относительные значения разницы МНК-средних составили соответственно -29,3% и -41,9% (p<0,0001 для обоих сезонов). Активная терапия ассоциировалась с лучшими показателями оценки «Опросника по качеству жизни при риноконъюнктивите» (RQLQ) в первом и втором сезонах пыления: относительные значения разницы МНК-средних составили соответственно -23,1% и -34,5%. Частота развившихся во время лечения нежелательных явлений (НЯВЛ) в группе 300 ИР СЛИТ не была выше по сравнению с группой плацебо и снижалась во втором сезоне (соответственно 70,7% и 64,0% пациентов в 1-м сезоне и 46,8% и 48,6% - во втором сезоне). Это снижение частоты НЯВЛ с течением времени наблюдалось также в связи с распространенными локальными нежелательными явлениями (НЯ), такими как оральный зуд (наблюдавшийся у 24,7% пациентов в группе СЛИТ в 1-м сезоне и у 8,3% во 2-м сезоне; в группе плацебо эта частота составила соответственно 3,8% и 0,8%). Эффективность лечения и риск развития НЯВЛ, по-видимому, не зависели от наличия или отсутствия орального аллергического синдрома [56].
В многоцентровом, ДСПК рандомизированном исследовании фазы III Wahn et al. [57] рандомизировали 207 детей в возрасте от 4 до 12 лет, страдавших АР/риноконъюнктивитом, вызванным пыльцой трав, в сочетании с бронхиальной астмой или без нее, в группу активной терапии (СЛИТ с использованием водного экстракта пыльцы шести трав) и группу плацебо. Применялась предсезонная и сезонная схема терапии. Основной конечной точкой эффективности было сравнение величины изменения площади под кривой симптомно-лекарственного индекса (symptom-medication score), начиная с исходного сезона до первого сезона пыления после начала лечения. Значения составили -212,5 и -97,8 в группе активной СЛИТ и группе плацебо соответственно (p<0,004), свидетельствуя о существенно более выраженном снижении тяжести заболевания в группе, получавшей активную СЛИТ. Что касается безопасности, то у 75,9% пациентов в группе активной терапии СЛИТ наблюдалось по меньшей мере одно НЯ (в сравнении с 32,7% пациентов в группе плацебо), однако тяжелых НЯ, связанных с лечением, зарегистрировано не было. В этом исследовании, однако, был изучен лишь один сезон пыления, следовательно, невозможно было оценить последствия прекращения и возобновления лечения.
В большинстве исследований предсезонной и сезонной схемы СЛИТ рассматривались лекарственные средства, созданные на основе пыльцы трав и березы, однако изучались и другие виды пыльцы. Например, Creticos et al. [58] изучили применение предсезонной и сезонной СЛИТ с использованием стандартизированного водного экстракта амброзии. Всего было рандомизировано 429 пациентов (группа активной СЛИТ: n=218, плацебо: n=211), принявших участие в многоцентровом ДСПК рандомизированном исследовании фазы III, проводившемся в Северной Америке. Терапия проводилась в период между апрелем 2011 года (то есть по меньшей мере за 4 месяца до начала периода распространения пыльцы амброзии - в октябре) и ноябрем 2011 года (то есть окончанием периода распространения пыльцы). Главной конечной точкой эффективности было среднее значение индекса, связывавшего ежедневные симптомы риноконъюнктивита и применение препаратов, на протяжении периода распространения пыльцы амброзии. В группе СЛИТ это значение (0,82±1,64) было значительно ниже, чем в группе плацебо (1,44±2,40; p<0,001). И в этом исследовании был изучен всего один сезон пыления, то есть возможность оценить последствия прекращения и возобновления отсутствовала.
Несмотря на то, что ДСПК РКИ остаются золотым стандартом при оценке экспериментальных лекарственных препаратов, исследования, проводимые в условиях «реальной клинической практики», имеют непревзойденное значение для достижения наиболее полной оценки эффективности и безопасности в целевой популяции пациентов в условиях, соответствующих практическому применению препаратов. С этой целью Hadler et al. в Германии провели открытое проспективное неинтервенционное исследование, оценив применение СЛИТ раствором на основе аллергенов пыльцы березы (300 ИР) у 716 пациентов с поливалентной и моновалентной аллергией (средний возраст ± SD: 38±16 лет; возрастной диапазон: 3-87) на протяжении двух сезонов распространения пыльцы [59]. Применялась схема предсезонной и сезонной терапии. Количественная оценка симптомов пациентов осуществлялась при помощи гибридной шкалы, при этом учитывались степень тяжести и частота возникновения симптомов только ринита, только конъюнктивита и риноконъюнктивита. Средняя величина индекса ринита в сезоне пыления березы перед исследованием составляла 4,83. Это значение снизилось до 3,17 в первом сезоне пыления и до 2,31 (снижение на 52%, p<0,001) во втором сезоне. Средний индекс конъюнктивита снизился с 3,74 до 2,1, а затем до 1,69 (снижение на 55%, p<0,001). Наконец, средний индекс риноконъюнктивита снизился с 3,76 до 2,29, а затем до 1,76 (снижение на 53%, p<0,001). При анализе подгрупп было показано, что применение СЛИТ раствором с аллергенами пыльцы (300 ИР) было в одинаковой степени эффективным у пациентов с моновалентной и поливалентной аллергией, так же как и у пациентов, начавших лечение в течение сезона пыльцы. Доля пациентов, требовавших применения симптоматических препаратов, в течение первого и второго сезонов распространения пыльцы была значительно ниже (p<0,001) (59% и 48% соответственно), в сравнении с 81% до исследования. Клиническое улучшение отмечалось как у пациентов с моновалентной аллергией, так и у лиц с поливалентной аллергией. Раствор аллергенов березовой пыльцы для СЛИТ (300 ИР) характеризовался хорошей переносимостью; 97% пациентов отметили «хорошую» или «очень хорошую» переносимость препарата. У девяноста процентов пациентов в течение двух сезонов терапии не отмечалось нежелательных явлений [59]. В клинической практике большинство пациентов, получавших сублингвальную терапию аллергенспецифичным раствором для СЛИТ (300 ИР), были удовлетворены лечением [60]; комплаентность и показатель возобновления рецептов были относительно высокими [55,61].
В совокупности эти данные практического использования раствора для СЛИТ (300 ИР) с аллергенами березовой пыльцы подтвердили результаты ДСПК РКИ.
Третьим основным типом лекарственных препаратов для АСИТ являются таблетки СЛИТ. На сегодняшний день для показания АР, индуцируемого травяной пыльцой (в сочетании с конъюнктивитом или без конъюнктивита), у взрослых и детей зарегистрировано две таблетированные лекарственные формы СЛИТ на основе травяной пыльцы (таблетки на основе аллергенов одной травы [36,37] и пяти трав [38,39]). Согласно информации, приведенной в соответствующей «Общей характеристике лекарственного препарата», и результатам базовых ДСПК РКИ, таблетки СЛИТ на основе аллергенов пыльцы одной травы со стандартизованным уровнем качества (СКТ) 75 000 SQ-T[36,37] одобрены для применения в рамках непрерывной круглогодичной схемы (начинающейся до первого сезона пыления; рисунок 1), тогда как таблетки СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) [38,39] зарегистрированы для использования в рамках прерывистой предсезонно-сезонной терапии (начинающейся за четыре месяца до предполагаемого начала сезона пыления и заканчивающейся в конце сезона; рисунок 1). Таким образом, общая длительность лечения в течение года составляет от 5 до 7 месяцев (в зависимости от продолжительности сезона цветения), при этом действие препаратов (по данным исследования в камере контролируемого воздействия аллергена) начинается к концу первого месяца терапии [62].
На протяжении последних 10 лет безопасность и/или эффективность предсезонной и сезонной терапии с использованием новых таблеток СЛИТ (300 ИР) на основе аллергенов пыльцы пяти трав неоспоримо доказаны в серии пред- и пострегистрационных клинических исследований, проводившихся как у взрослых пациентов, так и в детской популяции [39]. Всего 2 512 участников исследования в разных странах мира были рандомизированы в группы, получавшие либо таблетки СЛИТ на основе аллергенов пыльцы пяти трав (n=1 514), либо плацебо (n=998) [39]. Далее необходимо отметить, что таблетки СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) продемонстрировали сходную эффективность в различных клинических ситуациях (у пациентов с моновалентной и поливалентной сенсибилизацией, при высоком симптоматическом индексе и у пациентов с повышенной кожной чувствительностью) [63]. После проведения базового односезонного ДСПК РКС фазы II/III, в котором доза 300 ИР была отобрана для дальнейшего изучения и регистрации [64], Didier et al. в 5-летнем ДСПК РКИ, проводившемся в исследовательских центрах Европейского Союза и Канады, изучили вопрос о длительности сохранения эффекта таблеток СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) и эффективности после прекращения лечения у взрослых пациентов с АР [39,52,53]. Важно, что в настоящее время Европейское агентство по лекарственным средствам требует от препаратов для АСИТ выполнения следующих условий: 1) эффективность в первом сезоне после начала лечения; 2) доказанный стойкий клинический эффект (то есть поддержание существенной и клинически значимой эффективности на протяжении двух-трех лет терапии) и 3) долгосрочная эффективность (то есть устойчивая существенная и клинически значимая эффективность на протяжении нескольких лет после окончания лечения - болезнь-модифицирующий эффект) [65].
В соответствии с этим Didier et al. исследовали предсезонную и сезонную терапию таблетками СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) в течение трех сезонов у взрослых пациентов (от 18 до 50 лет) с анамнезом сезонного АР на пыльцу трав, наблюдавшегося на протяжении свыше двух сезонов пыления, и продолжали отслеживать состояние пациентов еще в течение двух сезонов после окончания лечения [39,52,53,66]. В общей сложности было рандомизировано 633 пациента, вошедших в три группы: 1) пациенты, получавшие таблетки СЛИТ на основе аллергенов пыльцы трав (300 ИР), начавшие активную терапию за 4 месяца (группа 4М) до предполагаемого начала сезона пыления и продолжавшие терапию на протяжении сезона пыления; 2) группа, получавшая терапию таблетками СЛИТ на основе аллергенов пыльцы трав (300 ИР), которая первоначально в течение 2 месяцев получала плацебо (начиная за 4 месяца до предполагаемого начала сезона пыления, для поддержания маскировки), а затем в течение 2 месяцев - активную терапию (группа 2М), и продолжала активное лечение на протяжении сезона пыления; и, наконец, 3) группа, получавшая плацебо, начиная за 4 месяца до ожидаемого сезона пыления и на протяжении всего сезона пыления. Эта прерывистая терапия в одном из трех вариантов осуществлялась на протяжении трех сезонов пыления (годы 1-3). После окончания третьего сезона терапии за пациентами еще в течение двух сезонов распространения пыльцы осуществлялось наблюдение (период без лечения - годы 4 и 5). Из 633 рандомизированных пациентов 457 завершили 3-летнюю терапию и 435 вошли в анализ эффективности (после лечения) на 4-м году исследования. Главной конечной точкой эффективности в этом исследовании был симптоматический индекс в течение третьего сезона цветения.
Дополнительными конечными точками являлись шесть отдельных симптоматических индексов риноконъюнктивита (чихание, ринорея, назальный зуд, заложенность носа, зуд глаз и слезотечение), средний индекс использования лекарственных препаратов и индекс RQLQ. На 4-м году в двух группах активной терапии значения симптоматических индексов были сходны между собой и существенно ниже, чем в группе плацебо. Значимая эффективность отмечалась также на 5-м году исследования [66]. При последующем анализе post hoc было показано, что МНК-среднее значение комбинированного индекса в группе, получавшей таблетки 300 ИР, было на 28,1% ниже, чем в группе плацебо (p=0,0478). Это свидетельствует о долгосрочной эффективности и болезнь-модифицирующем эффекте таблеток СЛИТ на основе аллергенов пыльцы 5 трав с 300 ИР. Разница между значениями МНК-средних в группах 4М и 2М не была статистически значимой. Профиль безопасности таблеток СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) на всем протяжении исследования согласовался с данными предшествующих сообщений, характеризуясь возникновением преимущественно легких, преходящих и локальных НЯ [39,52,53,67]. На протяжении первых трех сезонов терапии частота и степень тяжести НЯВЛ снижалась от года к году во всех трех группах лечения. В первом сезоне терапии наиболее распространенными НЯВЛ были зуд в полости рта (30% и 11,4% в группах активной терапии и плацебо соответственно), раздражение горла (15% и 3,7% соответственно) и отек рта (6% и 1,4% соответственно). В течение первого года терапии (в отличие от второго и третьего года лечения) частота случаев досрочного прекращения лечения вследствие НЯВЛ у пациентов, получавших препарат 300 ИР, была выше, чем в группе плацебо (7,2% в двух группах активной терапии и 1,4% в группе плацебо). В течение четвертого года исследования частота развившихся на фоне лечения НЯ в группах 300 ИР (4М), 300 ИР (2М) и плацебо была приблизительно одинаковой: 31,7%, 34,8% и 35,9% соответственно. Важно отметить, что обострение астмы не являлось существенной проблемой: один случай, имевший место в группе 300 ИР (4М), и два случая в группе плацебо были расценены как не имеющие связи с исследуемой терапией [52,53].
Вслед за вышеупомянутыми ДСПК РКИ многочисленные пострегистрационные исследования, проведенные в Европе, подтвердили безопасность и/или эффективность таблеток СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) при применении предсезонной и сезонной схемы терапии в повседневной клинической практике. В Германии в рамках многоцентрового проспективного открытого неинтервенционного исследования OPTIMAL была проведена оценка переносимости и эффективности схемы сезонно-предсезонной терапии таблетками СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) в течение двух лет подряд в общей сложности у 1 482 взрослых пациентов и детей (в том числе у 248 детей в возрасте от 4 до 11 лет и 201 подростка в возрасте от 12 до 17 лет) [68]. Средний индекс активности риноконъюнктивита в течение двух сезонов терапии был ниже, чем в течение сезона до начала лечения (соответственно на 51% и 64%; p<0,001). Важно отметить, что симптоматический индекс астмы у 522 пациентов, имевших легкую астму в числе сопутствующих заболеваний, на протяжении двух сезонов терапии также был ниже, чем на исходном уровне (на 60% и 70% соответственно в течение 1-го и 2-го года соответственно; p<0,001). При анализе только среди детей было показано, что средний индекс активности риноконъюнктивита снизился с 4,1 на исходном уровне до 1,93 после первого сезона терапии и до 1,39 после второго сезона. В подростковой группе соответствующие значения составили 4,05, 1,97 и 1,39. Средний индекс активности риноконъюнктивита снизился у пациентов как с моновалентной, так и с поливалентной аллергией, что подтверждает результаты ДСПК РКИ. Например, соответствующие значения индекса активности риноконъюнктивита на исходном уровне, после 1-го и после 2-го года терапии составили 4,05, 1,95 и 1,29 у детей с моновалентной аллергией и 4,09, 1,94 и 1,46 у детей с поливалентной аллергией [68].
Аналогичное многоцентровое открытое обсервационное одномоментное односезонное исследование пред- и сезонной терапии таблетками СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) было проведено в Испании [69]. Всего в это исследование вошло 226 взрослых пациентов (средний возраст: 33,9±11,5 лет). У пятидесяти пяти процентов пациентов имелась легкая астма, у 92% - персистирующий АР среднетяжелой степени (согласно критериям классификации «Аллергический ринит и его вклад в развитие астмы») [1,2]). После проведения предсезонно-сезонной терапии таблетками СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) доля пациентов со среднетяжелыми симптомами АР составила 30%. Снизилось также применение симптоматических лекарственных препаратов. Доля пациентов, применявших пероральные Н1-антигистаминные препараты и ИКС, снизилась соответственно с 92% и 77% на исходном уровне до 62% и 28% в конце периода терапии [69].
Пострегистрационный профиль безопасности таблеток СЛИТ на основе аллергенов пыльцы пяти трав
В Германии пострегистрационные исследования безопасности предсезонной и сезонной терапии таблетками СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) проводились у взрослых пациентов и у детей [39,59,60,70]. В одном исследовании, проводившемся в 354 исследовательских центрах в разных районах Германии, приняли участие 808 взрослых и 91 ребенок или подросток с АР и/или аллергическим конъюнктивитом, вызванными травяной пыльцой [39]. По завершении периода лечения, продолжавшегося 191 день, по меньшей мере одно НЯ было зарегистрировано у 320 пациентов (35,6%). Наиболее распространенными НЯ были парестезии в области рта (10,9% явлений), зуд в области рта (6,9%), раздражение горла (7,7%) и отек рта (5,3%). В результате НЯ 85 пациентов (9,5%) досрочно прервали лечение.
Еще в одном исследовании, проведенном в 207 исследовательских центрах, приняли участие 829 детей и подростков в возрасте от 5 до 17 лет [70]. По окончании периода лечения, средняя продолжительность которого составила 190 дней, у 218 пациентов (27,4%) было зарегистрировано по меньшей мере одно НЯ (главным образом раздражение горла (n=114), парестезии в области рта (n=49), зуд в области рта (n=39) и отек рта (n=37)). Наиболее серьезное НЯ (отек Квинке в области губ) произошло у пациента, который за год до этого перенес ангионевротический отек на фоне ПКИТ. Хорошую или очень хорошую переносимость лечения отметили 84,7% пациентов, 87,0% родителей и 89,7% лечащих врачей. В этих двух исследованиях не было зарегистрировано ни одного случая анафилаксии и применения адреналина [39,70]. Наконец, по данным 2-летнего исследования, основывавшегося на частоте возобновления рецептов на АСИТ на основе аллергенов травяной пыльцы, показатели приверженности лечению у пациентов, получавших СЛИТ, оказались значительно выше, чем у пациентов, получавших ПКИТ (p<0,02) [55]. Таким образом, предсезонная и сезонная (прерывистая) терапия таблетками СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) продемонстрировала благоприятный профиль эффективности и безопасности в реальной клинической практике.
Сравнение эффективности и безопасности предсезонно-сезонной и круглогодичной схем СЛИТ
Проведено несколько исследований, в которых выполнено прямое сравнение предсезонно-сезонной и круглогодичной схем терапии. Очевидно, проведение простых слепых или двойных слепых исследований проблематично, учитывая несомненное различие в длительности сравниваемых режимов лечения (если только пациенты в когортах предсезонно-сезонной терапии не будут в течение оставшейся части года получать плацебо). В исследовании Sieber et al. был проведен независимый метаанализ данных пациентов, принимавших участие в трех открытых проспективных обсервационных исследованиях стандартизированных препаратов СЛИТ на основе пыльцы растений семейства мятликовые или семейства березовые. Всего было изучено 1052 пациента с АР, вызванным пыльцой растений [61]. Цель исследования заключалась в непрямом сравнении круглогодичной терапии с сезонным лечением и сравнении сверхкороткого протокола титрования со стандартным титрованием дозы. В трех исследованиях применялся соответственно круглогодичный режим лечения с классическим титрованием дозы, сезонная терапия со сверхкоротким протоколом титрования и либо круглогодичная, либо сезонная схема лечения. Наиболее часто использовались препараты аллергенов, изготовленные из экстрактов пыльцы растений семейства березовые (49,9%) и растений семейства мятликовые (41,6%). Использование различных схем лечения ассоциировалось с улучшением симптоматических индексов и индексов использования лекарственных препаратов (при сравнении периода исследования с исходным периодом), причем значимых различий между вариантами терапии не отмечалось. Sieber et al. предположили, что эквивалентная эффективность сезонной и круглогодичной схем СЛИТ может иметь значение для ежегодной стоимости лечения, хотя показатель комплаентности в данном исследовании не оценивался [61].
Quercia провел прямое сравнительное исследование предсезонно-сезонной терапии с чисто предсезонной схемой лечения [71]. В качестве препарата СЛИТ использовалась таблетированная лекарственная форма мономерных карбамилированных аллергоидов из пыльцы трав. Было изучено три группы пациентов. Пациенты группы 1 получали таблетки, содержавшие 1 000 аллергенных единиц (AU), один раз в неделю в непрерывном режиме с ноября 2005 по июль 2007 года (то есть на протяжении двух сезонов пыления). Пациенты группы 2 получали по одной таблетке 1 000 AU пять раз в неделю только на протяжении 10-недельного предсезонного периода. В обеих группах СЛИТ отмечалось сходное и значимое уменьшение степени тяжести симптомов, оценивавшееся по визуальной аналоговой шкале, после первого и второго сезонов пыления, в сравнении с исходной выраженностью симптомов в группах 1 и 2, а также в сравнении с симптомами третьей группы пациентов (группы 3), получавших только симптоматическую терапию. Данное исследование имело ряд ограничений. Во-первых, в нем использовался открытый дизайн. Трудно, однако, организовать полностью двойное слепое контролируемое рандомизированное исследование, в котором часть пациентов (в отличие от остальных) должны на определенное время прекращать лечение. Во-вторых, исследуемые подгруппы были малочисленными (n=10, 11 и 11 в группах 1, 2 и 3 соответственно). В-третьих, пациенты 1-й и 2-й групп в течение предсезонного периода, предположительно играющего решающую роль, получали разные дозы аллергена (в расчете на неделю).
Прямые сравнительные исследования безопасности предсезонно-сезонной терапии по отношению к круглогодичному лечению не проводились. Тем не менее по данным базовых клинических исследований таблеток СЛИТ на основе аллергенов пыльцы трав, проводившихся в Европе и Северной Америке, лекарственные формы, включающие экстракты пыльцы одной травы или пяти трав, по-видимому, не имеют существенных различий в профиле безопасности. Nelson et al. [37] заметили, что, хотя нежелательные явления наблюдались у большинства взрослых пациентов и пациентов детского возраста (60-80%), получавших таблетки на основе экстракта пыльцы одной травы, эти явления в основном имели локальный и преходящий характер и оценивались как легкие или умеренные по степени тяжести. Наиболее распространенными локальными НЯ были зуд в области рта (наблюдавшийся у 32-54% пациентов, получавших активную терапию в разных исследованиях) и раздражение горла (у 9-37% пациентов). Системные нежелательные явления встречались редко [37]. Обобщая данные по безопасности таблеток на основе аллергенов пыльцы пяти трав, Didier et al. [39] использовали весьма близкие формулировки. Большинстве НЯ имели легкую или среднюю степень тяжести, при этом наиболее распространенными были зуд в области рта и раздражение горла (наблюдались более чем у 5% пациентов) [39]. Случаев смерти или анафилактических реакций в этих исследованиях не отмечалось.
В свете опубликованных данных можно заключить, что предсезонная и сезонная терапия с использованием препаратов СЛИТ с экстрактом березовой пыльцы 300 ИР и экстрактом пыльцы пяти трав 300 ИР доказала свою эффективность и безопасность. Основываясь на этом, можно задаться вопросом о том, имеет ли добавочную клиническую или экономическую ценность использование круглогодичных схем СЛИТ при лечении АР, вызванного пыльцой растений. Действительно, таблетки СЛИТ на основе аллергенов одной травы (75 000 SQ-T), зарегистрированные для проведения круглогодичной терапии, успешно применялись по незарегистрированным показаниям для предсезонно-сезонного лечения [72]. В многоцентровом проспективном открытом обсервационном исследовании, проведенном во Франции, 130 врачей осуществляли лечение 628 пациентов в среднем на протяжении 5,5 месяца в году (4 месяца в предсезонном периоде и затем в течение сезона пыления) на протяжении трех сезонов подряд. Данные по эффективности не приведены, поскольку главной целью исследования было изучение безопасности. Частота связанных с лечением НЯ в течение первого, второго и третьего года исследования составила соответственно 46,2%, 14,4% и 1,8%. Показатель комплаентности в течение первого года был равен 71,8%, на втором году - 86,8% и на третьем году - 90,3%, что служит дополнительным свидетельством хорошей комплаентности, отмечаемой при использовании предсезонно-сезонной схемы лечения [72]. Данные 934 пациентов, получавших лечение таблетками СЛИТ на основе аллергенов пыльцы одной травы (75 000 SQ-T), которые зарегистрированы для использования в качестве круглогодичной терапии, свидетельствуют о том, что для достижения клинической эффективности необходимо проводить лечение как минимум на протяжении 2 месяцев перед началом сезона пыления [54].
Взаимосвязь между дозой аллергена и схемой введения препаратов
Между поддерживающей дозой аллергена, клинической эффективностью и схемой терапии, вероятно, имеются определенные взаимосвязи. В настоящее время не вызывает сомнения существование связи «доза-ответ» при проведении АСИТ. В двенадцати из пятнадцати исследований подбора доз, рассмотренных в отчете рабочей группы по анализу взаимосвязей «доза-ответ» аллерген-специфической иммунотерапии Европейской академии аллергии и клинической иммунологии [73], сообщалось о наличии связи «доза-ответ» при оценке клинической эффективности. В связи с этим можно рассмотреть упоминавшиеся выше таблетки СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) и таблетки СЛИТ на основе аллергена пыльцы одной травы (75 000 SQ-T). В пересчете на стандартизированные единицы для экстрактов аллергенов, использование которых считает обязательным Управление по контролю качества лекарственных препаратов и пищевых продуктов США (FDA) (биоэквивалентная аллергенная единица - BAU, рассчитывается на основании реакции на внутрикожную пробу у высокочувствительных пациентов) [74], таблетки СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) содержат 9 000 BAU [75], а таблетки СЛИТ на основе аллергена пыльцы одной травы (75 000 SQ-T) содержат 2 800 BAU [76]. По данным собственных анализов соответствующих производителей, содержание основного аллергена (Phl p 5) в таблетках СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) составляет 25 мкг, а в таблетках СЛИТ на основе аллергена пыльцы одной травы (75 000 SQ-T) - 15 мкг [64,77]. Несмотря на то, что эти таблетки различаются по значению BAU и содержанию основного аллергена (для оптимального сравнения эти параметры следует оценивать в одной и той же лаборатории, у одних и тех же пациентов и с использованием одних и тех же реактивов [74,78]), они, по-видимому, обеспечивают достижение сходного эффекта в течение первого года терапии, о чем свидетельствуют результаты исследований III фазы (в которых величина эффекта оценивалась по значению индекса активности риноконъюнктивита в сравнении с плацебо) [36-39]. Рассматривая предсезонно-сезонную схему терапии таблетками на основе аллергенов пыльцы трав, можно отметить, что устойчивая эффективность и эффективность после окончания лечения в первом сезоне подтверждена только для лекарственной формы на основе аллергенов пыльцы пяти трав (300 ИР) [39]. Кроме того, по данным базового РКИ по изучению диапазона доз, низкодозированные (100 ИР) таблетки СЛИТ на основе аллергенов пыльцы пяти трав не превосходят по эффективности плацебо [64].
Медико-экономические аспекты предсезонной и сезонной схемы лечения
Предсезонно-сезонная схемы терапии характеризуются преимуществами перед круглогодичными схемами в плане экономических параметров и комплаентности. Во-первых, меньшая длительность лечения при использовании прерывистых схем подразумевает, что пациенты получают меньшее количество препарата, что приводит к уменьшению затрат на лекарственные препараты. В двух исследованиях была проведена оценка экономической эффективности предсезонной и сезонной СЛИТ при АР, вызванном пыльцой трав [79,80].
Westerhout et al. предприняли анализ экономической эффективности 3-летней предсезонно-сезонной терапии таблетками СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) (в дополнение к симптоматической терапии (СТ)) на протяжении 9-летнего временного интервала в сравнении со следующими вариантами лечения: 1) круглогодичной СЛИТ таблетками на основе экстракта пыльцы одной травы (в дополнение к СТ); 2) круглогодичной схемой ПКИТ (в дополнение к СТ) и 3) только СТ (то есть стандартным лечением) при лечении АР, вызванного пыльцой трав, с точки зрения системы здравоохранения Германии [79]. Эффективность терапии оценивалась на основании непрямого сравнения, проведенного в рандомизированных клинических исследованиях (РКИ), в которых в качестве обычного препарата сравнения использовалось плацебо (в частности, стандартная терапия). Кроме того, был проведен метаанализ РКИ, изучавших эти три варианта лечения. Это позволило оценить эффективность каждого вида лечения по сравнению с плацебо (стандартной терапии) в плане уменьшения выраженности симптомов АР и увеличения числа бессимптомных дней. Результаты исследования показали, что прирост стоимости в расчете на год жизни с поправкой на качество жизни (QALY), в сравнении с исключительно симптоматической терапией, составил €14 728 при использовании СЛИТ на основе пыльцы 5 трав (300 ИР), при этом прирост стоимости был равен €1 356, а прирост QALY - 0,092. Полученное в результате соотношение эффективности добавочных затрат находилось ниже общепринятых в Европе пороговых значений. Между тем экономия добавочных затрат при использовании таблеток СЛИТ на основе аллергенов пыльцы пяти трав по отношению к круглогодичной терапии таблетками СЛИТ на основе аллергена пыльцы одной травы или круглогодичной ПКИТ составила соответственно €1 142 и €54, а соответствующие инкременты QALY составляли 0,015 и 0,027. Эти результаты показывают, что в Германии у пациентов с аллергическим ринитом, вызванным пыльцой трав, таблетки СЛИТ на основе аллергенов пыльцы 5 трав для предсезонно-сезонной терапии представляют собой более экономически выгодный вариант лечения (по сравнению с таблетками СЛИТ на основе аллергена пыльцы одной травы для круглогодичной терапии, круглогодичной ПКИТ и симптоматической терапией). Однако углубленный анализ чувствительности показал, что выводы, сделанные из этой модели, могут находиться под влиянием неопределенности оценок эффективности терапии [79].
В недавно проведенном экономическом исследовании [80] был выполнен анализ минимизации затрат, основанный на систематическом обзоре 20 ДСПК исследований сезонного АР, вызванного пыльцой трав. Были изучены следующие четыре схемы лекарственной терапии (с точки зрения канадской системы здравоохранения): 1) предсезонно-сезонная терапия таблетками СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) с применением СТ при необходимости; 2) круглогодичная СЛИТ таблетками на основе аллергена пыльцы одной травы; 3) круглогодичная ПКИТ; и 4) предсезонная и сезонная ПКИТ. Результаты показали, что предсезонно-сезонная терапия таблетками СЛИТ на основе пыльцы пяти трав (300 ИР) характеризуется как минимум не меньшей эффективностью, сходной безопасностью и меньшими годичными затратами на лечение в сравнении с круглогодичной или сезонной ПКИТ и круглогодичной СЛИТ таблетками на основе аллергенов пыльцы одной травы [80]. На протяжении первого года лечения предсезонное и сезонное применение таблеток СЛИТ на основе аллергенов пыльцы пяти трав (300 ИР) в сочетании с СТ ассоциировалось со значительной экономией затрат, в сравнении с круглогодичной ПКИТ (2 471 канадских долларов), сезонной ПКИТ (948 канадских долларов) и круглогодичной СЛИТ таблетками на основе аллергенов пыльцы одной травы (1 168 канадских долларов) [80].
Выводы
При лечении АР, вызванного пыльцой растений, прерывистые схемы СЛИТ по меньшей мере столь же эффективны и безопасны, как круглогодичные схемы СЛИТ, судя по показателям устойчивости эффекта на протяжении нескольких сезонов пыления и даже после окончания лечения. Необходимо провести прямые сравнительные исследования для оценки снижения затрат на лечение при использовании прерывистых схем СЛИТ, а также для получения доказательств улучшения комплаентности или безопасности по сравнению с круглогодичными режимами СЛИТ. Анализ предсезонной и сезонной прерывистых схем показал, что лекарственная форма, содержащая аллергены пыльцы пяти трав (300 ИР), представляет собой единственную таблетированную форму СЛИТ, для которой программа клинической разработки подтвердила краткосрочную, устойчивую и посттерапевтическую эффективность.
Сокращения
НЯ: нежелательное явление;
АСИТ: аллергенспецифическая иммунотерапия;
АР: аллергический ринит;
BAU: биоэквивалентная аллергенная единица;
ДСПК: двойное слепое, плацебо-контролируемое;
ИКС: интраназальный кортикостероид;
IgE: иммуноглобулин E;
ИР: индекс реактивности;
МНК: метод наименьших квадратов;
М: месяц;
QALY: год жизни с поправкой на качество жизни;
РКИ: рандомизированное клиническое исследование;
RQLQ: «Опросник по качеству жизни при риноконъюнктивите» (Rhinoconjunctivitis quality of Life Questionnaire);
ПКИТ: подкожная иммунотерапия;
СТ: симптоматическая терапия;
СЛИТ: сублингвальная иммунотерапия;
СЛ: стандарт лечения;
SQ-T: таблетки стандартизированного качества (Standardized quality tablet);
НЯВЛ: нежелательное явление, возникшее во время лечения.
Конфликт интересов
Pascal Demoly является консультантом и лектором компаний Stallergenes, ALK-Abello и Chiesi, ранее (в 2010-2014 гг.) являлся лектором компаний Merck, Astra Zeneca, Menarini и GlaxoSmithKline. Moises A. Calderon является платным консультантом, получает гонорар за лекции и/или пользуется спонсорской помощью при проведении исследований от компаний ALK-Abello, Merck, Stallergenes и Allergopharma. Thomas B. Casale ранее являлся лектором компании Stallergenes, был консультантом компании Circassia и использовал исследовательские гранты, предоставляемые его университету компаниями Merck, Stallergenes и Circassia. Hans-Jørgen Malling служил платным консультантом, получал гонорары за лекции и/или спонсорскую помощь при проведении исследований от компаний ALK-Abello (Дания), Stallergenes (Франция), Biomar (Австрия), Anergis (Швейцария) и HAL (Нидерланды). Ulrich Wahn служил платным консультантом, получал гонорары за лекции и/или спонсорскую помощь при проведении исследований от компании Stallergenes.
Вклад авторов публикации
PD, MAC, TBC, HJM и UW внесли существенный вклад в поиск, разбор и анализ литературы. PD, MAC, TBC, HJM и UW участвовали в написании чернового варианта рукописи и/или критическом рассмотрении рукописи с точки зрения важнейших интеллектуальных аспектов ее содержания. Все авторы одобрили заключительный вариант работы, представленный для опубликования.
Благодарности
Мы благодарим David Fraser, PhD, за помощь в качестве медицинского автора.
Сведения об авторах
Аллергологическое подразделение, отделение пульмонологии, больница Арно де Вильнев, университетская клиника Монпелье, Монпелье, Франция. 2 Университет Сорбонны, Университет Пьера и Мари Кюри Париж 06, Национальный институт здравоохранения и медицинских исследований (INSERM), объединенная группа научных исследований (UMR-S) 1136, Институт эпидемиологии и здравоохранения им. Пьера Луи (IPLESP), группа по изучению эпидемиологии аллергических и респираторных заболеваний, Париж, Франция. 3Отделение аллергологии и клинической иммунологии, Имперский колледж Лондона - NHLI, Больница Ройал Бромптон, Лондон, Великобритания. 4Отделение внутренних болезней, колледж Морсани, Медицинский университет Южной Флориды, Тампа, шт. Флорида, Омаха, шт. Небраска, США. 5 Клиника аллергологии, университетская больница Гентофте, Копенгаген, Дания. 6 Отделение детской пульмонологии и иммунологии, больница Шарите им. Вирхова, университет им. Гумбольдта, Берлин, Германия.
Получена: 18 декабря 2014 г., принята в печать: 23 марта 2015 г.
Опубликована онлайн: 04 мая 2015 г.
Список литературы
1. Bousquet J, Khaltaev N, Cruz AA, Denburg J, Fokkens WJ, Togias A, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) 2008 Update (in collaboration with the World Health Organization, GA2LEN and AllerGen). Allergy. 2008;63:S8-160.
2. Brozek JL, Bousquet J, Baena-Cagnani CE, Bonini S, Canonica GW, Casale TB, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) guidelines: 2010 revision. J Allergy Clin Immunol. 2010;126:466-76.
3. Shaaban R, Zureik M, Soussan D, Neukirch C, Heinrich J, Sunyer J, et al. Rhinitis and onset of asthma: a longitudinal population-based study. Lancet. 2008;372:1049-57.
4. Kessler RC, Almeida DM, Berglund P, Stang P. Pollen and mold exposure impairs the work performance of employees with allergic rhinitis. Ann Allergy Asthma Immunol. 2001;87:289-95.
5. Meltzer EO. Quality of life in adults and children with allergic rhinitis. J Allergy Clin Immunol. 2001;108:545-53.
6. Leger D, Annesi-Maesano I, Carat F, Rugina M, Chanal I, Pribil C, et al. Allergic rhinitis and its consequences on quality of sleep. An unexplored area. Arch Intern Med. 2006;166:1744-8.
7. Canonica GW, Bousquet J, Mullol J, Scadding GK, Virchow JC. A survey of the burden of allergic rhinitis in Europe. Allergy. 2007;62 Suppl 85:17-25.
8. Nathan RA. The burden of allergic rhinitis. Allergy Asthma Proc. 2007;28:3-9.
9. Valovirta E, Myrseth SE, Palkonen S. The voice of the patients: allergic rhinitis is not a trivial disease. Curr Opin Allergy Clin Immunol. 2008;8:1-9.
10. Meltzer EO, Bukstein DA. The economic impact of allergic rhinitis and current guidelines for treatment. Ann Allergy Asthma Immunol. 2011 ;106:S12-6.
11. Arbes Jr SJ, Gergen PJ, Elliott L, Zeldin DC. Prevalences of positive skin test responses to 10 common allergens in the US population: results from the third National Health and Nutrition Examination Survey. J Allergy Clin Immunol. 2005;116:377-83.
12. Bousquet PJ, Castelli C, Daures JP, Heinrich J, Hooper R, Sunyer J, et al. Assessment of allergen sensitization in a general population-based survey (European Community Respiratory Health Survey I). Ann Epidemiol. 2010;20:797-803.
13. Smith M, Jäger S, Berger U, Sikoparija B, Hallsdottir M, Sauliene I, et al. Geographic and temporal variations in pollen exposure across Europe. Allergy. 2014;69:913-23.
14. D'Amato G, Cecchi L, Bonini S, Nunes C, Annesi-Maesano I, Behrendt H, et al. Allergenic pollen and pollen allergy in Europe. Allergy. 2007;62:976-90.
15. Shea KM, Truckner RT, Weber RW, Peden DB. Climate change and allergic disease. J Allergy Clin Immunol. 2008;122:443-53.
16. Ziska L, Knowlton K, Rogers C, Dalan D, Tierney N, Elder MA, et al. Recent warming by latitude associated with increased length of ragweed pollen season in central North America. Proc Natl Acad Sci USA. 2011;108:4248-51.
17. Wallace DV, Dykewicz MS, Bernstein DI, Blessing-Moore J, Cox L, Khan DA, et al. The diagnosis and management of rhinitis: an updated practice parameter. J Allergy Clin Immunol. 2008;122(2):S1 -84.
18. Ramirez LF, Urbinelli R, Allaert FA, Demoly P. Combining H1-antihistamines and nasal corticosteroids to treat allergic rhinitis in general practice. Allergy. 2011;66:1501-2.
19. Migueres M, Fontaine JF, Haddad T, Grosclaude M, Saint-Martin F, Bem David D, et al. Characteristics of patients with respiratory allergy in France and factors influencing immunotherapy prescription: a prospective observational study (REALIS). Int J Immunopathol Pharmacol. 2011;24:387-400.
20. Canonica GW, Bousquet J, Casale T, Lockey RF, Baena-Cagnani CE, Pawankar R, et al. Sub-lingual immunotherapy: World Allergy Organization Position Paper 2009. Allergy. 2009;64 Suppl 91:1-59.
21. Canonica GW, Cox L, Pawankar R, Baena-Cagnani CE, Blaiss M, Bonini S, et al. Sublingual immunotherapy: World Allergy Organization position paper 2013 update. World Allergy Organ J. 2014;7:6.
22. Cox L, Nelson H, Lockey R, Calabria C, Chacko T, Finegold I, et al. Allergen immunotherapy: a practice parameter third update. J Allergy Clin Immunol. 2011;127(Suppl):S1-55.
23. Viswanathan RK, Busse WW. Allergen immunotherapy in allergic respiratory diseases: from mechanisms to meta-analyses. Chest. 2012;141:1 303- 14.
24. Matricardi PM, Kuna P, Panetta V, Wahn U, Narkus A. Subcutaneous immunotherapy and pharmacotherapy in seasonal allergic rhinitis: a comparison based on meta-analyses. J Allergy Clin Immunol. 2011;128:791-9.
25. Devillier P, Dreyfus JF, Demoly P, Calderón MA. A meta-analysis of sublingual allergen immunotherapy and pharmacotherapy in pollen-induced seasonal allergic rhinoconjunctivitis. BMC Med. 2014;12:71.
26. Eng PA, Borer-Reinhold M, Heijnen IA, Gnehm HP. Twelve-year follow-up after discontinuation of preseasonal grass pollen immunotherapy in childhood. Allergy. 2006;61:198-201.
27. Burks AW, Calderon MA, Casale T, Cox L, Demoly P, Jutel M, et al. Update on allergy immunotherapy: American Academy of Allergy, Asthma & Immunology / European Academy of Allergy and Clinical Immunology / PRACTALL consensus report. J Allergy Clin Immunol. 2013;131:1288-96.
28. Jacobsen L, Niggemann B, Dreborg S, Ferdousi HA, Halken S, Host A, et al. Specific immunotherapy has long-term preventive effect of seasonal and perennial asthma: 10-year follow-up on the PAT study. Allergy. 2007;62:943-8.
29. Calderon MA, Alves B, Jacobson M, Hurwitz B, Sheikh A, Durham S. Allergen injection immunotherapy for seasonal allergic rhinitis. Cochrane Database Syst Rev. 2007;1, CD001936.
30. Di Bona D, Plaia A, Scafidi V, Leto-Barone MS, Di Lorenzo G. Efficacy of sublingual immunotherapy with grass allergens for seasonal allergic rhinitis: a systematic review and meta-analysis. J Allergy Clin Immunol. 2010;126:558-66.
31. Calderon M, Mösges R, Hellmich M, Demoly P. Towards evidence-based medicine in specific grass pollen immunotherapy. Allergy. 2010;65:420-34.
32. Radulovic S, Wilson D, Calderon M, Durham S. Systematic reviews of sublingual immunotherapy (SLIT). Allergy. 2011;66:740-52.
33. Calderon MA, Penagos M, Sheikh A, Canonica GW, Durham S. Sublingual immunotherapy for treating allergic conjunctivitis. Cochrane Database Syst Rev. 2011;7, CD007685.
34. Calderon MA, Casale TB, Nelson HS, Demoly P. An evidence-based analysis of house dust mite allergen immunotherapy: a call for more rigorous clinical studies. J Allergy Clin Immunol. 2013;132:1322-36.
35. Lin SY, Erekosima N, Kim JM, Ramanathan M, Suarez-Cuervo C, Chelladurai Y, et al. Sublingual immunotherapy for the treatment of allergic rhinoconjunctivitis and asthma: a systematic review. JAMA. 2013;309:1278-88.
36. Senna GE, Calderon M, Milani M. Allergy immunotherapy tablet: Grazax® for the treatment of grass pollen allergy. Expert Rev Clin Immunol. 2011;7:21-7.
37. Nelson H, Lehmann L, Blaiss MS. Treatment of seasonal allergic rhinoconjunctivitis with a once-daily SQ-standardized grass allergy immunotherapy tablet. Curr Med Res Opin. 2012;28:1043-51.
38. Lyseng-Williamson K. Sublingual five-grass pollen tablets (Oralair®): a guide to their use as allergen immunotherapy for grass pollen-induced allergic rhinoconjunctivitis. Drugs Ther Perspec. 2014;30:200-8.
39. Didier A, Wahn U, Horak F, Cox LS. Five-grass-pollen sublingual immunotherapy tablet for the treatment of grass-pollen-induced allergic rhinoconjunctivitis: 5 years of experience. Expert Rev Clin Immunol. 2014;10:1309-24.
40. Kannan JA, Epstein TG. Immunotherapy safety: what have we learned from surveillance surveys? Curr Allergy Asthma Rep. 2013;13:381-8.
41. Lockey RF, Benedict LM, Turkeltaub PC, Bukantz SC. Fatalities from immunotherapy (IT) and skin testing (ST). J Allergy Clin Immunol. 1987;79:660-77.
42. Bousquet J, Lockey R, Malling HJ, Alvarez-Cuesta E, Canonica GW, Chapman MD, et al. Allergen immunotherapy: therapeutic vaccines for allergic diseases. World health organization. American academy of allergy, asthma and immunology. Ann Allergy Asthma Immunol. 1998;81:401-5.
43. Alvarez-Cuesta E, Bousquet J, Canonica GW, Durham SR, Malling HJ, Valovirta E, et al. Standards for practical allergen-specific immunotherapy. Allergy. 2006;61(82):1 -20.
44. Calderón MA, Simons FE, Malling HJ, Lockey RF, Moingeon P, Demoly P. Sublingual allergen immunotherapy: mode of action and its relationship with the safety profile. Allergy. 2012;67:302-11.
45. Lombardi C, Incorvaia C, Braga M, Senna G, Canonica GW, Passalacqua G. Administration regimens for sublingual immunotherapy to pollen allergens: what do we know? Allergy. 2009;64:849-54.
46. Palma-Carlos AG, Santos AS, Branco-Ferreira M, Pregal AL, Palma-Carlos ML, Bruno ME, et al. Clinical efficacy and safety of preseasonal sublingual immunotherapy with grass pollen carbamylated allergoid in rhinitic patients. A double-blind, placebo-controlled study. Allergol Immun (Madr). 2006;34:194-8.
47. Vervloet D, Birnbaum J, Laurent P, Hugues B, Fardeau MF, Massabie-Bouchat YP, et al. Safety and efficacy of Juniperus ashei sublingual-swallow ultra-rush pollen immunotherapy in cypress rhinoconjunctivitis. A double-blind, placebo-controlled study. Int Arch Allergy Immunol. 2007;142:239-46.
48. Ott H, Sieber J, Brehler R, Fölster-Holst R, Kapp A, Klimek L, et al. Efficacy of grass pollen sublingual immunotherapy for three consecutive seasons and after cessation of treatment: the ECRIT study. Allergy. 2009;64:1394-401.
49. Bufe A, Ziegler-Kirbach E, Stoeckmann E, Heidemann P, Gehlhar K, Holland-Letz T, et al. Efficacy of sublingual swallow immunotherapy in children with severe grass pollen allergic symptoms: a double-blind placebo-controlled study. Allergy. 2004;59:498-504.
50. Sabate E: Adherence to long-term therapies: evidence for action. Available from: http://www.who.int/chp/knowledge/publications/adherence_report/ en/ [Last accessed 22 January 2015]
51. Christensen AJ. Patient adherence to medical treatment regimens: bridging the gap between behavioral science and biomedicine. Current Perspectives In Psychology. New Haven: Yale University Press; 2004.
52. Didier A, Worm M, Horak F, Sussman G, de Beaumont O, Le Gall M, et al. Sustained 3-year efficacy of pre- and coseasonal 5-grass-pollen sublingual immunotherapy tablets in patients with grass pollen-induced rhinoconjunctivitis. J Allergy Clin Immunol. 2011;128:559-66.
53. Didier A, Malling HJ, Worm M, Horak F, Sussman G, Melac M, et al. Post-treatment efficacy of discontinuous treatment with 300IR 5-grass pollen sublingual tablet in adults with grass pollen-induced allergic rhinoconjunctivitis. Clin Exp Allergy. 2013;43:568-77.
54. Calderon MA, Birk AO, Andersen JS, Durham SR. Prolonged preseasonal treatment phase with Grazax sublingual immunotherapy increases clinical efficacy. Allergy. 2007;62:958-61.
55. Sieber J, De Geest S, Shah-Hosseini K, Mösges R. Medication persistence with long-term, specific grass pollen immunotherapy measured by prescription renewal rates. Curr Med Res Opin. 2011;27:855-61.
56. Worm M, Rak S, de Blay F, Malling HJ, Melac M, Cadic V, et al. Sustained efficacy and safety of a 300IR daily dose of a sublingual solution of birch pollen allergen extract in adults with allergic rhinoconjunctivitis: results of a double-blind, placebo-controlled study. Clin Transl Aller. 2014;4:7.
57. Wahn U, Klimek L, Ploszczuk A, Adelt T, Sandner B, Trebas-Pietras E, et al. High-dose sublingual immunotherapy with single-dose aqueous grass pollen extract in children is effective and safe: a double-blind, placebo-controlled study. J Allergy Clin Immunol. 2012;130:886-93. e5. doi:10.1016/j.jaci.2012.06.047.
58. Creticos PS, Esch RE, Couroux P, Gentile D, D’Angelo P, Whitlow B, et al. Randomized, double-blind, placebo-controlled trial of standardized ragweed sublingual-liquid immunotherapy for allergic rhinoconjunctivitis. J Allergy Clin Immunol. 2014;133:751-8. 10.1016/j.jaci.2013.10.041.
59. Hadler M, Karagiannis E, Shah-Hosseini K, Mösges R. Effectiveness and tolerability of a 2-year sublingual allergen immunotherapy (AIT) in routine medical practice in birch pollen allergic patients. Allergy: Eur J Allergy Clin Immunol. 2013;68 Suppl 97:483.
60. Hadler M, Schnitzer S, Schnitker J, Sieber J. Treatment satisfaction with sublingual immunotherapy in a real-life setting. World Aller Organ J. 2012;5 Suppl 2:S67.
61. Sieber J, Köberlein J, Mösges R. Sublingual immunotherapy in daily medical practice: effectiveness of different treatment schedules - IPD meta-analysis. Curr Med Res Opin. 2010;26:925-32.
62. Horak F, Zieglmayer P, Zieglmayer R, Lemell P, Devillier P, Montagut A, et al. Early onset of action of a 5-grass-pollen 300IR sublingual immunotherapy tablet evaluated in an allergen challenge chamber. J Allergy Clin Immunol. 2009;124:471-7.
63. Malling HJ, Montagut A, Melac M, Patriarca G, Panzner P, Seberova E, et al. Efficacy and safety of 5-grass pollen sublingual immunotherapy tablets in patients with different clinical profiles of allergic rhinoconjunctivitis. Clin Exp Allergy. 2009;39:387-93.
64. Didier A, Malling HJ, Worm M, Horak F, Jäger S, Montagut A, et al. Optimal dose, efficacy, and safety of once-daily sublingual immunotherapy with a 5-grass pollen tablet for seasonal allergic rhinitis. J Allergy Clin Immunol. 2007;120:1338-45.
65. Committee for Medicinal Products for Human Use at the European Medicines Agency. Guideline on the clinical development of products for specific immunotherapy for the treatment of allergic diseases, Draft CHMP/EWP/18504/2006. London: 2008.
66. ORALAIR Sweet Vernal, Orchard, Perennial Rye, Timothy, and Kentucky Blue Grass Mixed Pollens Allergen Extract Tablet for Sublingual Use: food and Drug Administration Allergenic Products Advisory Committee Briefing Document. Stallergenes S.A., 2013. Available from: www.fda.gov/downloads/ AdvisoryCommittees/CommitteesMeetingMaterials/ BloodVaccinesandOtherBiologics/AllergenicProductsAdvisoryCommittee/ UCM377851.pdf [Last accessed 22 January 2014]
67. Halken S, Agertoft L, Seidenberg J, Bauer CP, Payot F, Martin-Muñoz MF, et al. Five-grass pollen 300IR SLIT tablets: efficacy and safety in children and adolescents. Pediatr Allergy Immunol. 2010;21:970-6.
68. Karagiannis E, Shah-Hosseini K, Hadler M, Mösges R. PD14 - Non- interventional 2-year study of sublingual immunotherapy in children and adolescents with allergic rhinoconjunctivitis caused by grass pollen. Clin Trans Aller. 2014;4 Suppl 1:14.
69. Antolin D, Valbuena T, Valls A, Garrido S, Blanco C, Garcia MA. One season of treatment with 5 grass pollen tablets in adults demonstrated a reduction in disease symptoms and impacts: findings of the SMILE study. Allergy: Eur J Allergy Clin Immunol. 2013;68 Suppl 97:479.
70. Eberle P, Brueck H, Gall R, Hadler M, Sieber J, Karagiannis E: An observational, real- life safety study of a 5-grass-pollen sublingual tablet in children and adolescents. Pediatr Allergy Immunol. 2014 Nov 7. doi:10.1111/pai.12298.
71. Quercia O, Bruno ME, Compalati E, Falagiani P, Mistrello G, Stefanini GF. Efficacy and safety of sublingual immunotherapy with grass monomeric allergoid: comparison between two different treatment regimens. Eur Ann Allergy Clin Immunol. 2011;43:176-83.
72. Wessel F, Chartier A, Meunier JP, Magnan A. Safety and tolerability of an SQ- standardized GRAss ALlergy immunotherapy tablet (GRAZAX®) in a real-life setting for three consecutive seasons - the GRAAL trial. Clin Drug Investig. 2012;32:451-63.
73. Calderón MA, Larenas D, Kleine-Tebbe J, Jacobsen L, Passalacqua G, Eng PA, et al. European Academy of Allergy and Clinical Immunology task force report on 'dose-response relationship in allergen-specific immunotherapy’. Allergy. 2011;66:1345-59.
74. Larenas-Linnemann D, Cox LS, Immunotherapy and Allergy Diagnostics Committee of the American Academy of Allergy, Asthma and Immunology. European allergen extract units and potency: review of available information. Ann Allergy Asthma Immunol. 2008;100:137-45.
75. Prescribing information for ORALAIR in the US. Available from: http:// dailymed.nlm.nih.gov/dailymed/fda/fdaDrugXsl.cfm?setid=854c9772-63b9- 44a3-a11e-77b29c59e91d&type=display [Last accessed 22 January 2015]
76. FDA Briefing Document. Biologic License Application (BLA) for Timothy Grass Pollen Allergen Extract Tablet for Sublingual Use. Available from: http://www.fda.gov/downloads/advisorycommittees/ committeesmeetingmaterials/bloodvaccinesandotherbiologics/ allergenicproductsadvisorycommittee/ucm378092.pdf [Last accessed 22 January 2015]
77. Durham SR, Yang WH, Pedersen MR, Johansen N, Rak S. Sublingual immunotherapy with once-daily grass allergen tablets: a randomized controlled trial in seasonal allergic rhinoconjunctivitis. J Allergy Clin Immunol. 2006;117:802-9.
78. Larenas-Linnemann D, Esch R, Plunkett G, Brown S, Maddox D, Barnes C, et al. Maintenance dosing for sublingual immunotherapy by prominent European allergen manufacturers expressed in bioequivalent allergy units. Ann Allergy Asthma Immunol. 2011;107:448-58.
79. Westerhout KY, Verheggen BG, Schreder CH, Augustin M. Cost effectiveness analysis of immunotherapy in patients with grass pollen allergic rhinoconjunctivitis in Germany. J Med Econ. 2012;15:906-17.
80. Dranitsaris G, Ellis AK. Sublingual or subcutaneous immunotherapy for seasonal allergic rhinitis: an indirect analysis of efficacy, safety and cost. J Eval Clin Pract. 2014;20:225-38.
